Termodinamika
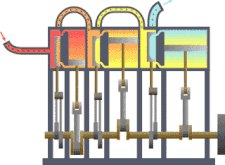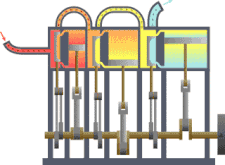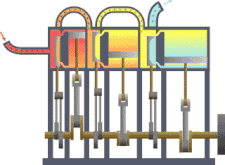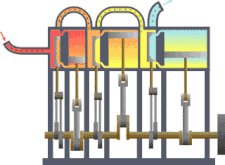
Sebuah sistem termodinamika
Termodinamika (
bahasa Yunani:
thermos = 'panas' and
dynamic = 'perubahan') adalah
fisika energi ,
panas,
kerja,
entropi dan kespontanan proses. Termodinamika berhubungan dekat dengan
mekanika statistik di mana banyak hubungan termodinamika berasal.
Pada sistem di mana terjadi proses perubahan wujud atau pertukaran energi, termodinamika klasik tidak berhubungan dengan
kinetika reaksi
(kecepatan suatu proses reaksi berlangsung). Karena alasan ini,
penggunaan istilah "termodinamika" biasanya merujuk pada termodinamika
setimbang. Dengan hubungan ini, konsep utama dalam termodinamika adalah
proses kuasistatik, yang diidealkan, proses "super pelan". Proses termodinamika bergantung-waktu dipelajari dalam
termodinamika tak-setimbang.
Karena termodinamika tidak berhubungan dengan konsep
waktu, telah diusulkan bahwa termodinamika setimbang seharusnya dinamakan termostatik.
Hukum termodinamika kebenarannya sangat umum, dan hukum-hukum ini
tidak bergantung kepada rincian dari interaksi atau sistem yang
diteliti. Ini berarti mereka dapat diterapkan ke sistem di mana
seseorang tidak tahu apa pun kecual perimbangan transfer energi dan
wujud di antara mereka dan lingkungan. Contohnya termasuk perkiraan
Einstein tentang
emisi spontan dalam
abad ke-20 dan riset sekarang ini tentang
termodinamika benda hitam.
Konsep dasar dalam termodinamika
Pengabstrakkan dasar atas termodinamika adalah pembagian dunia
menjadi sistem dibatasi oleh kenyataan atau ideal dari batasan. Sistem
yang tidak termasuk dalam pertimbangan digolongkan sebagai lingkungan.
Dan pembagian sistem menjadi subsistem masih mungkin terjadi, atau
membentuk beberapa sistem menjadi sistem yang lebih besar. Biasanya
sistem dapat diberikan keadaan yang dirinci dengan jelas yang dapat
diuraikan menjadi beberapa parameter !
Sistem termodinamika
Sistem termodinamika adalah bagian dari
jagat raya
yang diperhitungkan. Sebuah batasan yang nyata atau imajinasi
memisahkan sistem dengan jagat raya, yang disebut lingkungan.
Klasifikasi sistem termodinamika berdasarkan pada sifat batas
sistem-lingkungan dan perpindahan materi, kalor dan entropi antara
sistem dan lingkungan.
Ada tiga jenis sistem berdasarkan jenis pertukaran yang terjadi antara sistem dan lingkungan:
- sistem terisolasi: tak terjadi pertukaran panas, benda atau kerja
dengan lingkungan. Contoh dari sistem terisolasi adalah wadah
terisolasi, seperti tabung gas terisolasi.
- sistem tertutup: terjadi pertukaran energi (panas dan kerja) tetapi tidak terjadi pertukaran benda dengan lingkungan. Rumah hijau
adalah contoh dari sistem tertutup di mana terjadi pertukaran panas
tetapi tidak terjadi pertukaran kerja dengan lingkungan. Apakah suatu
sistem terjadi pertukaran panas, kerja atau keduanya biasanya
dipertimbangkan sebagai sifat pembatasnya:
- pembatas adiabatik: tidak memperbolehkan pertukaran panas.
- pembatas rigid: tidak memperbolehkan pertukaran kerja.
- sistem terbuka: terjadi pertukaran energi (panas dan kerja) dan
benda dengan lingkungannya. Sebuah pembatas memperbolehkan pertukaran
benda disebut permeabel. Samudra merupakan contoh dari sistem terbuka.
Dalam kenyataan, sebuah sistem tidak dapat terisolasi sepenuhnya dari
lingkungan, karena pasti ada terjadi sedikit pencampuran, meskipun
hanya penerimaan sedikit penarikan
gravitasi. Dalam analisis sistem terisolasi, energi yang masuk ke sistem sama dengan energi yang keluar dari sistem.
Keadaan termodinamika
Ketika sistem dalam keadaan seimbang dalam kondisi yang ditentukan, ini disebut dalam keadaan pasti (atau keadaan sistem).
Untuk keadaan termodinamika tertentu, banyak sifat dari sistem
dispesifikasikan. Properti yang tidak tergantung dengan jalur di mana
sistem itu membentuk keadaan tersebut, disebut fungsi keadaan dari
sistem. Bagian selanjutnya dalam seksi ini hanya mempertimbangkan
properti, yang merupakan fungsi keadaan.
Jumlah properti minimal yang harus dispesifikasikan untuk menjelaskan keadaan dari sistem tertentu ditentukan oleh
Hukum fase Gibbs. Biasanya seseorang berhadapan dengan properti sistem yang lebih besar, dari jumlah minimal tersebut.
Pengembangan hubungan antara properti dari keadaan yang berlainan dimungkinkan.
Persamaan keadaan adalah contoh dari hubungan tersebut.
Hukum-hukum Dasar Termodinamika
Terdapat empat Hukum Dasar yang berlaku di dalam sistem termodinamika, yaitu:
- Hukum Awal (Zeroth Law) Termodinamika
-
- Hukum ini menyatakan bahwa dua sistem dalam keadaan setimbang dengan
sistem ketiga, maka ketiganya dalam saling setimbang satu dengan
lainnya.
- Hukum Pertama Termodinamika
-
- Hukum ini terkait dengan kekekalan energi. Hukum ini menyatakan perubahan energi dalam dari suatu sistem termodinamika tertutup sama dengan total dari jumlah energi kalor yang disuplai ke dalam sistem dan kerja yang dilakukan terhadap sistem.
- Hukum kedua Termodinamika
-
- Hukum kedua termodinamika terkait dengan entropi. Hukum ini
menyatakan bahwa total entropi dari suatu sistem termodinamika
terisolasi cenderung untuk meningkat seiring dengan meningkatnya waktu,
mendekati nilai maksimumnya.
- Hukum ketiga Termodinamika
Hukum ketiga termodinamika terkait dengan
temperatur nol absolut.
Hukum ini menyatakan bahwa pada saat suatu sistem mencapai temperatur
nol absolut, semua proses akan berhenti dan entropi sistem akan
mendekati nilai minimum. Hukum ini juga menyatakan bahwa entropi benda
berstruktur kristal sempurna pada temperatur nol absolut bernilai nol.